Jak działa nowoczesna szczepionka na raka? Fakty, mechanizmy, skuteczność, najnowsze doniesienia naukowe.
Wstęp
W ostatnich miesiącach świat nauki i medycyny odnotował znaczący, bezprecedensowy postęp w rozwoju szczepionek przeciwnowotworowych. Obiecujące wyniki uzyskane w badaniach klinicznych, szczególnie w zakresie szczepionek opartych o technologię mRNA oraz innych platform genetycznych i białkowych, dają realną nadzieję na skuteczniejszą walkę z najbardziej złośliwymi typami nowotworów. Współczesna onkologia coraz bardziej skupia się na spersonalizowanej immunoterapii, która pozwala na precyzyjne i celowane leczenie nowotworów przy jednoczesnym ograniczeniu skutków ubocznych. Poniższy artykuł prezentuje najbardziej aktualne, szczegółowe i usystematyzowane informacje na temat postępów w tej dziedzinie, ze szczególnym uwzględnieniem przełomowych badań z 2025 roku i światowego kontekstu rozwoju tej terapii.
Mechanizm działania nowoczesnych szczepionek przeciwnowotworowych
Personalizacja immunoterapii i indywidualizacja leczenia raka
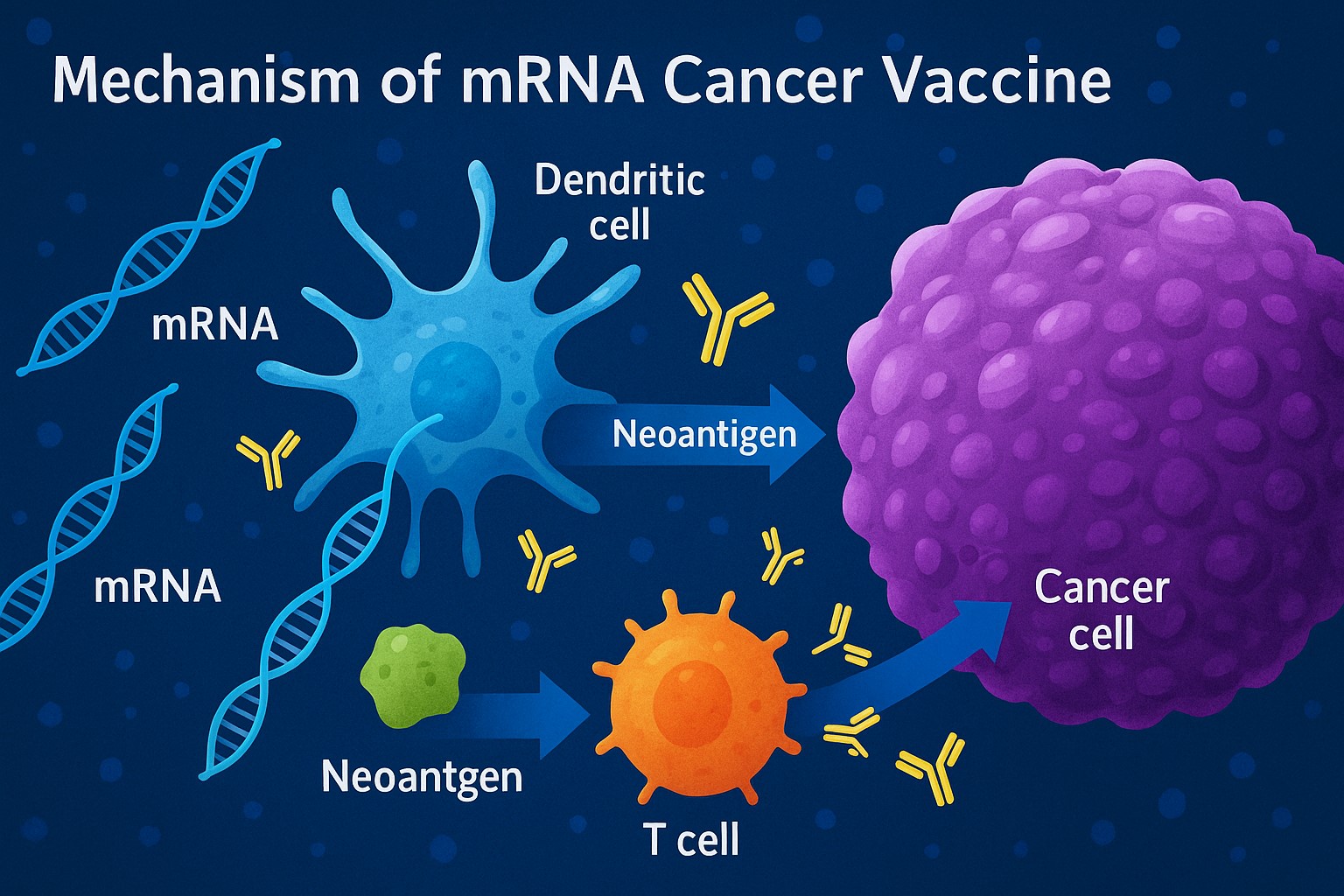
Nowoczesne szczepionki przeciwnowotworowe opierają się na coraz bardziej zaawansowanym podejściu do leczenia nowotworów, w którym analiza materiału genetycznego guza konkretnego pacjenta pozwala na identyfikację tzw. neoantygenów, czyli unikalnych białek powstających w wyniku mutacji nowotworowych. Na tej podstawie projektowana jest indywidualna szczepionka, która stymuluje układ odpornościowy pacjenta do rozpoznania i zniszczenia komórek nowotworowych, przy jednoczesnym zachowaniu tolerancji wobec zdrowych tkanek. Spersonalizowana immunoterapia obejmuje nie tylko szczepionki, ale także przeciwciała monoklonalne, inhibitory punktów kontrolnych oraz komórki CAR-T, jednak szczepionki mRNA stanowią obecnie najdynamiczniej rozwijany obszar tej gałęzi medycyny.
Technologia mRNA w immunoonkologii
Szczepionki mRNA, znane szeroko z walki z pandemią COVID-19, znalazły nowe i rewolucyjne zastosowanie w terapii nowotworów. W szczepionkach tych wykorzystywany jest informacyjny RNA kodujący wybrane antygeny nowotworowe, które po podaniu do organizmu są syntetyzowane przez komórki gospodarza. Powstające białka są rozpoznawane przez układ immunologiczny, co prowadzi do aktywacji limfocytów T i skierowania ich działania przeciwko nowotworowi. Kluczową zaletą tej technologii jest możliwość szybkiego zaprojektowania preparatu pod konkretny przypadek kliniczny, co pozwala na indywidualizację leczenia każdego pacjenta. W ostatnich latach obserwuje się także rozwój szczepionek opartych o inne platformy, takie jak białka rekombinowane, peptydy, a nawet szczepionki komórkowe i wektorowe.
Immunogenność i bezpieczeństwo szczepionek przeciwnowotworowych
Szczepionki przeciwnowotworowe, w szczególności te oparte o mRNA, charakteryzują się wysoką immunogennością, czyli zdolnością do silnej aktywacji komórek układu odpornościowego. Badania przedkliniczne i kliniczne potwierdzają, że preparaty te są stosunkowo bezpieczne – najczęściej obserwuje się łagodne, przemijające reakcje miejscowe, objawy grypopodobne oraz bardzo rzadko poważniejsze powikłania autoimmunologiczne. Współczesne szczepionki przeciwnowotworowe są również w stanie wywołać długotrwałą pamięć immunologiczną, co istotnie zmniejsza ryzyko nawrotów nowotworu.
Najnowsze badania kliniczne – przełomowe osiągnięcia 2025 roku
Szczepionka na raka nerki – szczepionka personalizowana (Dana-Farber Cancer Institute & Yale Cancer Center)
W badaniu klinicznym fazy I, opublikowanym w 2025 roku przez zespoły z Dana-Farber Cancer Institute i Yale Cancer Center, dziewięciu pacjentów z zaawansowanym rakiem nerki (stadium III i IV) otrzymało indywidualnie zaprojektowane szczepionki na podstawie zaawansowanej analizy DNA i RNA ich nowotworów. Po ponad 34 miesiącach obserwacji u wszystkich pacjentów zaobserwowano brak nawrotu choroby. Jest to unikatowy wynik w tej grupie chorych, u których standardowa terapia wiąże się z wysokim ryzykiem wznowy nowotworu. Szczepionka była bardzo dobrze tolerowana – najczęstsze działania niepożądane miały charakter łagodny, ograniczały się do objawów grypopodobnych i reakcji miejscowych. Ten sukces stanowi pierwsze tak jednoznaczne potwierdzenie wysokiej skuteczności spersonalizowanej szczepionki mRNA w zaawansowanym nowotworze litym, otwierając drogę do dalszych badań z większą grupą pacjentów oraz rozwoju podobnych rozwiązań dla innych nowotworów litych.
Szczepionka na raka trzustki – autogene cevumeran (BioNTech & Genentech)
Rak trzustki uznawany jest za jeden z najtrudniejszych do leczenia i najbardziej agresywnych nowotworów, charakteryzujący się bardzo wysoką śmiertelnością. W 2025 roku przedstawiono wyniki fazy I badań klinicznych nad szczepionką mRNA autogene cevumeran, opracowaną przez konsorcjum BioNTech i Genentech. U szesnastu pacjentów po chirurgicznym usunięciu guza podano spersonalizowane szczepionki. Silną odpowiedź immunologiczną zaobserwowano u ośmiu osób, a u sześciu z nich nie doszło do nawrotu choroby po trzech latach. Dla porównania, standardowe leczenie daje znacznie gorsze wyniki długoterminowe. Szczepionka była bardzo dobrze tolerowana – działania niepożądane ograniczały się do objawów przejściowych i łagodnych. Wyniki te otwierają drogę do kolejnych, bardziej zaawansowanych faz badań klinicznych (faza II już się rozpoczęła), a skuteczność oraz bezpieczeństwo terapii zostały potwierdzone przez niezależne zespoły badawcze na całym świecie. Co istotne, platforma autogene cevumeran umożliwia szybkie dopasowanie terapii do indywidualnych potrzeb pacjenta, co jest kluczowe przy tak agresywnym nowotworze.
Szczepionka na czerniaka – mRNA-4157/V940 (Moderna & Merck)
Czerniak jest jednym z najlepiej poznanych immunologicznie nowotworów, dzięki czemu od lat pozostaje w centrum badań nad szczepionkami. Wieloośrodkowe badanie fazy IIb (KEYNOTE-942) objęło pacjentów z wysokim ryzykiem nawrotu czerniaka. Spersonalizowana szczepionka mRNA-4157/V940, podawana w skojarzeniu z pembrolizumabem (inhibitor punktu kontrolnego, Keytruda), zmniejszyła ryzyko nawrotu aż o 44% w porównaniu do monoterapii immunologicznej. Osiągnięcie to zaowocowało przyznaniem szczepionce statusu terapii przełomowej (Breakthrough Therapy) przez amerykańską FDA i otwiera drogę do rejestracji oraz szerokiego, komercyjnego zastosowania. Warto dodać, że szczepionka mRNA-4157/V940 wykazała także korzystny profil bezpieczeństwa i dobre wyniki w analizach farmakoekonomicznych, co może przyspieszyć proces jej wdrożenia do praktyki klinicznej na całym świecie.
Inne nowotwory – perspektywy badań
Obecnie prowadzone są intensywne badania nad szczepionkami mRNA oraz innymi platformami w licznych typach nowotworów: rak płuca, rak piersi, glejak, rak prostaty, chłoniaki, nowotwory głowy i szyi oraz raki przewodu pokarmowego. W badaniach przedklinicznych i wczesnych fazach klinicznych uzyskano już pierwsze sygnały wysokiej immunogenności oraz korzystnego profilu bezpieczeństwa. Coraz większą uwagę poświęca się także strategiom łączącym szczepionki z innymi terapiami celowanymi, immunoterapią i chemioterapią. Zwiększa to potencjał leczenia i daje nadzieję na skuteczność również w nowotworach dotychczas uznawanych za „zimne” immunologicznie.
Wyzwania i bariery w upowszechnieniu szczepionek przeciwnowotworowych
Koszty, produkcja i logistyka
Największym wyzwaniem dla spersonalizowanych szczepionek przeciwnowotworowych pozostaje koszt ich produkcji oraz logistyka dostarczania indywidualnych preparatów w krótkim czasie od rozpoznania nowotworu. Każda szczepionka wymaga osobnego procesu projektowania, syntezy oraz walidacji, co znacząco wpływa na jej cenę i dostępność na szeroką skalę. Ponadto, procesy produkcji szczepionek mRNA są ściśle kontrolowane pod względem jakości, bezpieczeństwa oraz stabilności preparatu. Firmy biotechnologiczne i systemy ochrony zdrowia na całym świecie pracują nad rozwiązaniami automatyzującymi te procesy i obniżającymi koszty, w tym nad wdrożeniem platform cyfrowych do analizy sekwencji nowotworów i szybkiego projektowania terapii.
Długofalowa skuteczność i bezpieczeństwo
Kluczowe pozostaje długofalowe monitorowanie pacjentów przez wiele lat po podaniu szczepionek, by ocenić trwałość odpowiedzi immunologicznej i wykluczyć ryzyko późnych powikłań, takich jak autoagresja czy powikłania ze strony narządów niebędących celem terapii. W badaniach obserwacyjnych zbierane są dane dotyczące reakcji późnych, efektów ubocznych i jakości życia pacjentów. Współpraca międzynarodowa oraz sieci rejestrów klinicznych mają kluczowe znaczenie dla szybkiego identyfikowania potencjalnych problemów oraz doskonalenia terapii.
Regulacje, proces rejestracji i wyzwania etyczne
Szczepionki przeciwnowotworowe wymagają rygorystycznych procedur zatwierdzających. Organy rejestracyjne na całym świecie, takie jak FDA (USA), EMA (Unia Europejska) czy PMDA (Japonia), analizują dane dotyczące bezpieczeństwa, skuteczności oraz korzyści klinicznych, zanim dopuszczą szczepionkę do rutynowego stosowania. Dodatkowym wyzwaniem są kwestie etyczne związane z dostępnością terapii, sprawiedliwą dystrybucją oraz transparentnością procesów decyzyjnych. Dyskusja publiczna oraz udział pacjentów w projektowaniu badań klinicznych stają się coraz ważniejszym elementem całego procesu wdrażania innowacyjnych terapii.
Wpływ postępów technologicznych i cyfryzacji
Rozwój technologii sztucznej inteligencji, big data oraz platform bioinformatycznych rewolucjonizuje cały proces projektowania, produkcji i monitorowania szczepionek przeciwnowotworowych. Dzięki nowym narzędziom możliwe jest szybsze identyfikowanie neoantygenów, automatyczna synteza sekwencji mRNA oraz przewidywanie potencjalnych skutków ubocznych. Cyfrowe bazy danych i rejestry chorych umożliwiają śledzenie długoterminowych efektów leczenia na skalę globalną.
Przyszłość terapii przeciwnowotworowych – nowa era onkologii?
Eksperci przewidują, że już w ciągu najbliższych kilku lat pierwsze szczepionki przeciwnowotworowe trafią do szerokiego zastosowania klinicznego, szczególnie w nowotworach o wysokim ryzyku nawrotu i niewielkiej skuteczności dotychczasowych terapii. Spersonalizowana immunoterapia, w tym szczepionki mRNA, może stać się przełomem w leczeniu nowotworów, poprawiając przeżywalność i jakość życia pacjentów. Kluczowe znaczenie będzie miała współpraca międzynarodowa, rozwój sieci badań klinicznych oraz inwestycje w innowacje technologiczne. Prognozuje się, że w perspektywie dekady szczepionki na bazie mRNA oraz inne platformy genetyczne staną się podstawą leczenia i profilaktyki wielu typów nowotworów, w tym tych o najgorszym rokowaniu.
Warto podkreślić, że przyszłość terapii onkologicznych zależy nie tylko od postępu w dziedzinie nauk podstawowych, ale również od skuteczności translacji odkryć do codziennej praktyki klinicznej oraz systemowego wsparcia dla pacjentów. Integracja wiedzy z zakresu biologii molekularnej, genetyki, immunologii oraz medycyny cyfrowej stwarza szansę na rewolucyjne zmiany w leczeniu raka na świecie. Wieloośrodkowe badania i inicjatywy międzynarodowe, takie jak Cancer Moonshot, przyspieszają rozwój nowych terapii oraz zwiększają dostępność innowacyjnych rozwiązań dla chorych w różnych regionach globu.
Podsumowanie – czy istnieje skuteczna szczepionka na raka?
Obiecujące wyniki badań z 2025 roku dają realną nadzieję na skuteczne, bezpieczne i coraz bardziej dostępne leczenie nowotworów z wykorzystaniem nowoczesnych szczepionek. Sukcesy w czerniaku, raku nerki i raku trzustki potwierdzają potencjał tej technologii, a trwające badania mogą w najbliższych latach zrewolucjonizować onkologię na świecie. Rosnąca liczba pacjentów korzystających z innowacyjnych terapii, coraz lepsze wyniki długoterminowe oraz ograniczenie skutków ubocznych pozwalają patrzeć w przyszłość z ostrożnym optymizmem. Istotnym aspektem pozostaje jednak równość w dostępie do terapii, dalszy rozwój infrastruktury medycznej oraz wsparcie dla badań podstawowych i translacyjnych. Tylko synergiczne działanie środowisk naukowych, klinicznych i systemów ochrony zdrowia umożliwi pełne wykorzystanie potencjału szczepionek przeciwnowotworowych.
Źródła naukowe i dalsza lektura
- Nature, Science, New England Journal of Medicine – aktualne publikacje z 2025
- Komunikaty FDA, EMA, WHO
- New kidney cancer vaccine puts 9 advance-stage patients into remission
- Autogene cevumeran – Wikipedia
- mRNA-4157/V940 – Wikipedia
- Cancer Moonshot Initiative
- Raporty globalnych rejestrów badań klinicznych
- Opracowania FDA, EMA i PMDA dotyczące rejestracji szczepionek genetycznych

















Szczepionki przeciwnowotworowe oparte na technologii mRNA mogą w przyszłości współgrać z terapiami opartymi na mikrobiomie jelitowym, co może dodatkowo zwiększać skuteczność leczenia nowotworów. Najnowsze badania wykazują, że skład mikroflory jelitowej istotnie wpływa na odpowiedź immunologiczną pacjenta i potencjalnie może modulować efektywność szczepionek oraz immunoterapii. W kilku ośrodkach badawczych trwają już prace nad precyzyjnym doborem probiotyków i diety wspomagającej leczenie onkologiczne. W przyszłości oczekuje się zintegrowanych strategii leczenia, uwzględniających zarówno indywidualny profil genetyczny guza, jak i kompozycję mikrobioty. Taki model może doprowadzić do powstania spersonalizowanych schematów leczenia, opartych na interdyscyplinarnych badaniach molekularnych.